
Back Van der Waals se krag Afrikaans قوى فان دير فالس Arabic Van-der-Vaals qüvvələri Azerbaijani Сілы Ван-дэр-Ваальса Byelorussian Сили на Ван дер Ваалс Bulgarian ভ্যানডার ওয়ালস বন্ধন Bengali/Bangla Van der Waalsove sile BS بەندی ڤان دەر ڤۆلس CKB Van der Waalsovy síly Czech Van der Waals-kræfter Danish
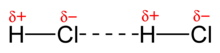
Les forces de van der Waals són forces atractives o repulsives febles entre entitats moleculars, o entre grups dins d'una mateixa entitat molecular, diferents de les de formació d'enllaç químic (covalent, iònic o metàl·lic) o de les interaccions electroestàtiques entre ions o grups d'ions i molècules neutres. Es divideixen en tres tipus:
Les forces de van der Waals són més febles que els enllaços químics que uneixen àtoms en els composts químics. Tanmateix, tenen un paper fonamental en moltes substàncies, per exemple, determinen el caràcter químic dels composts orgànics i la seva solubilitat en dissolvents polars i no polars. Són emprades a molts camps de la ciència i de la tecnologia: química orgànica, química inorgànica, química supramolecular, biologia estructural, ciència dels materials, ciència de les superfícies, nanotecnologia, física de la matèria condensada, etc.
- ↑ McNaught, A.D.; Wilkinson, A. IUPAC. Compendium of Chemical Terminology, the "Gold Book" (en anglès). 2a edició. Oxford: Blackwell Scientific Publications, 1997. DOI 10.1351/goldbook.V06597. ISBN 0-9678550-9-8 [Consulta: 11 novembre 2030].
© MMXXIII Rich X Search. We shall prevail. All rights reserved. Rich X Search